Висилати виконані завдання* та отримати консультацію, поділитися своїми досягненнями можна у Вайбері (0965753303) та за допомогою електронної пошти (nazarenko_innochka@ukr.net) з 9:00 по 14:00 (СБ, НД – вихідні)
Вчитель хімії – Назаренко Інна Валеріївна
*Велике прохання підписувати надіслані матеріали (ім’я, прізвище дитини/батьків)
з 04.05 по 22.05 діти повторюють вивчений матеріал у ІІ семестрі і поступово, виконують контрольні роботи, які знаходяться ТУТ
7-мі класи
- Повторити пар. 21,22.
- Робота з презентацією: Узагальнення знань з теми «Кисень. Повітря». (див. посилання)
- Виконати тестові завдання з третього або четвертого слайду (на вибір). Кожне завдання – 2б., всього 12 б. Завдання з останнього слайду – письмово.
8 клас
- Повторити пар. 19-22.
- Відео: Розв’язування задач на визначення молекул (дивитися за посиланням) https://www.youtube.com/watch?v=9lnYkPSUwAY
- Розв’язати задачі:
- Вирахувати число атомів Фосфору у фосфорі кількістю речовини 7 моль.
- Вирахувати об’єм метану CH3 масою 120 г.
- Вирахувати масу гідроген хлориду HCl об’ємом 179,2 л.
- Вирахуйте відносну густину SiF4 за азотом.
Кожне завдання – 3 б.
9 клас
- Повторити пар. 3-6.
- Відео: Розв’язування задач за темою «Розчини» (переглянути за посиланням) https://www.youtube.com/watch?v=ZR4ZfBn9tHs
- Розв’язати задачі:
Задача 1. Визначте масу води, в якій необхідно розчинити 50 г калій сульфату для одержання розчину з масовою часткою речовини 10%.
Задача 2. До розчину нітратної кислоти масою 200 г з масовою часткою кислоти 20% долили 50 мл води. Обчисліть масову частку нітратної кислоти в утвореному розчині.
- Готуємось до контрольного тестування за темою «Розчини».
10 клас
- Повторити пар. 26-29.
- Відео «Розв’язування задач за темами «Вуглеводні. Спирти» (переглянути відео за посиланням) https://www.youtube.com/watch?v=EJXuKHqyLK8
- Розв’язати задачу.
- Калій масою 4,7 грам помістили в етанол. Який об’єм (н.у.) водню виділиться?
- Готуємось до контрольного тестування з теми «Органічні речовини»

Дистанційне навчання тижня 27.04 – 30.04
7-мі класи
- Опрацювати пар.24. Повторити пар. 18-20.
- Відеоурок «Колообіг Оксигену в природі» https://www.youtube.com/watch?v=6YAkqK_QFWc
- Виконати завдання 179, с.146 (письмово)
8 клас
- Опрацювати пар. 22. Повторити пар. 20,21.
- Переглянути відео «Що таке відносна густина газів»
3. Переглянути презентацію “Відносна густина газів” за посиланням (ЗАВАНТАЖИТИ ТУТ)
4. Розв’язати задачі з презентації (останній слайд).
9 клас
- Опрацювати пар. 12.
- Відео «Якісні реакції на деякі йони» https://www.youtube.com/watch?v=NoWPtT08D44
- Виконати завд. 82, с.61
- Повторити пар. 7,8.
10 клас
- Повторити пар. 19-25.
- Відео «Вуглеводні» https://www.youtube.com/watch?v=9InzjIbyXCE
- Виконати тестові завдання. (ЗАВАНТАЖИТИ ТУТ)
Тестова перевірка знань з теми: «Насичені та ненасичені вуглеводні»
Завдання з вибором однієї правильної відповіді
1. Позначте загальну формулу алкенів:
A) СnН2n-6; Б) СnН2n-2; В) CnH2n ; Г) СnH2n+2;
2. Позначте елемент-органоген:
А) Са; Б) Со; В) С; Г) К
3. Позначте формулу гексану:
А) С6Н12; Б) С6Н14; В) С7Н14; Г) С6Н
4. Позначте сполуку, яка здатна полімеризуватися:
А) етан; Б) етилен; В) метан; Г) етиловий спирт.
5. Позначте загальну формулу алканів:
A) СnН2n-2; Б) СnН2n+4; В) CnH2n-6 Г) СnH2n+2
6. Позначте молекулярну формулу пропену;
А) С4Н10; Б)С3Н6; В) С3Н8; Г)С2Н6,
7. Позначте, який вуглеводень знебарвлює розчин калій перманганату:
А) метан; Б) пропан; В) гексан; Г) етен.
8. Позначте формулу октану:
А) С4Н10; Б) С9Н20; В) С8Н16; Г) С8Н18.
Завдання з вибором кількох правильних відповідей
9. Позначте гомологи пропену:
А) С6H14; Б) С6Н12; В) С2H4; Г) С5Н10.
Завдання на встановлення відповідності
10. Установіть відповідність між назвою речовини та її формулою:
| Назва речовини | Формула речовини |
| А) бутан; | 1) СН3—СН2—СН2—СН3; |
| Б) пропен; | 2) СН≡СН; |
| В) етин; | З) СН2= СН—СН3; |
4)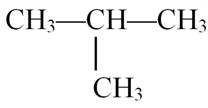 |

Дистанційна робота тижня 21.04 – 24.04
7-мі класи
- Опрацювати пар. 23
- Переглянути презентацію за посиланням “Маркування небезпечних речовин”
- Виконати вправу «Вірю-не вірю» ( +або -), відповісти на 12 питань (кожне 1 б.), відповіді відіслати на електронну пошту або Viber.
8 клас
- Опрацювати пар. 21.
- Переглянути відео «Пояснення розв’язування задач на знаходження молярної маси, маси, кількості речовини» https://www.youtube.com/watch?v=itDETNqJ_i0 з 14 хвилини до кінця.
- Переглянути презентацію за посиланням “Кількість речовин. Молярна маса. Молярний об’єм”. Розв’язати задачі з останнього слайду.
9 клас.
- Повторити пар. 11.
- Виконати завдання з презентації за посиланням (ЗАВАНТАЖИТИ ТУТ).
10 клас.
- Опрацювати пар. 34.
- Переглянути презентацію за посиланням “Значення природних і синтетичних сполук”, розв’язати задачі з останнього слайду.

Дистанційне навчання тижня 13.04 – 17.04
7-мі класи
- Переглянути відео «Складання рівнянь хімічних реакцій»
- Повторити пар. 19.
- Виконати завдання (ЗАВАНТАЖИТИ ТУТ)
8 клас
- Переглянути відео «Пояснення розв’язування задач на знаходження молярної маси, маси, кількості речовини» https://www.youtube.com/watch?v=itDETNqJ_i0 з початку до 14 хвилини.
- Переглянути презентацію “Молярна маса” ТУТ
- Опрацювати пар. 20, завд. 146 (усно), с. 109.
- Розв’язати задачі:
- Яка кількість речовини міститься в 180 г води ?
- Яку масу матиме мідна деталь, кількість речовини Купруму у якій 25,6 моль?
- У якій кількості води міститься стільки молекул, скільки їх у 3,92 г сульфатної кислоти H2SO4? *
9 клас
- Опрацювати пар. 10
- Переглянути відео « Складання рівнянь іонного обміну»
3. Переглянути відеодослід «Реакція йонного обміну» https://www.youtube.com/watch?v=nZ0dIXsb5sE
4. Виконати завдання 74 (а,б) , с. 57; 76( в,г), с. 57.
10 клас
- Переглянути відео «Природні органічні речовини» https://www.youtube.com/watch?v=WYV3Jbtj3eU
- Переглянути презентацію «Природні та синтетичні органічні речовини» ТУТ
- Опрацювати пар. 35. Виконати тестові завдання (ЗАВАНТАЖИТИ ТУТ)

Дистанційне навчання тижня 06.04 – 10.04
7-мі класи
- Повторити пар. 21,22. Виконати тестові завдання з теми: «Кисень». (ЗАВАНТАЖИТИ ТУТ)
Відео «Хімічні властивості кисню»
8 клас
- Опрацювати пар. 19.
Відео «Кількість речовини»
- Виконати завдання 130( усно), с.103; завд. 132 (письмово), с. 103.
9 клас
- Опрацювати пар. 8
Презентація « Сильні та слабкі електроліти. Ступінь дисоціації електролітів».
- Виконати завдання 57 (усно), с. 46; завд. 61, с. 47
10 клас
- Опрацювати пар. 33.
Відео «Якісна реакція на білки».
- Виконати завдання 240 (усно), 242 (письмово), с.190

ДИСТАНЦІЙНЕ НАВЧАННЯ ТИЖНЯ 30.03 – 03.04
7 клас
Хімія
Опрацювати пар. 22, виконати завдання 168 (усно),с. 136; завдання 170, с.136
Відеодослід «Горіння речовин» https://www.youtube.com/watch?v=VULlO7zgA9w
8 клас
Хімія
Виконати контрольні завдання по темі «Хімічний зв’язок» (завантажити текстовий файл)
8 Клас
Контрольна робота по темі:
«Хімічний зв’язок і будова речовини»
| Варіант І | Варіант ІІ |
| 1. (1 бал) Ковалентним називають хімічний зв’язок, що утворюється:
А) йонами; Б) спільною електронною парою; В) йонами та спільною електронною парою. |
1. (1 бал) Йонним називають хімічний зв’язок, що утворюється:
А) електростатичним притяганням між йонами; Б) спільною електронною парою; В) йонами та спільною електронною парою. |
| 2. (1 бал) У вузлах йонних кристалічних ґраток розміщені:
А) позитивно заряджені йони металів; Б) негативно заряджені йони металів; В) позитивно заряджені йони металів і негативно заряджені йони неметалів. |
2. (1 бал) У вузлах молекулярних кристалічних ґраток розміщені:
А) неполярні або полярні молекули; Б) атоми; В) позитивно заряджені йони металів і негативно заряджені йони неметалів. |
| 3. (1 бал) Вкажіть сполуку з ковалентним полярним зв’язком:
А) SO2; Б) H2; В) NaCl; Г) CaF2. |
3. (1 бал) Вкажіть сполуку з йонним зв’язком:
А) SO2; Б) Cl2; В) BaCl2; Г) HBr. |
| 4. (1 бал) Молекулярну кристалічну ґратку має:
А) NaCl; Б) PH3; В) C (алмаз); Г) CaO. |
4. (1 бал) Йонну кристалічну ґратку має:
А) KCl; Б) NH3; В) OF2; Г) F2. |
| 5. (2 бали) Укажіть вид хімічного зв’язку та тип кристалічної ґратки в наступних сполуках:
Au, MgCl2, Br2, P2O3. |
5. (2 бали) Укажіть вид хімічного зв’язку та тип кристалічної ґратки в наступних сполуках:
Ag, Na2S, I2, Mn2O3. |
| 6. (3 бали) Складіть електронні та графічні формули молекул, та поясніть утворення хімічного зв’язку в наступних сполуках:
OF2, CH4, PF5. |
6. (3 бали) Складіть електронні та графічні формули молекул, та поясніть утворення хімічного зв’язку в наступних сполуках:
SF6, SiH4, H2S. |
| 7. (3 бали) Елемент головної підгрупи ІV групи утворює летку сполуку з Гідрогеном, масова частка цього елемента в якій 87,5 %. Визначте цей елемент, укажіть формулу його вищого оксиду та формулу леткої сполуки з гідрогеном. В цих формулах визначте тип хімічного зв’язку та намалюйте структурну формулу. | 7. (3 бали) Елемент головної підгрупи І групи утворює вищій оксид з Оксигеном, масова частка цього елемента в якому 74,2 %. Визначте цей елемент, укажіть формулу його вищого оксиду. Визначте тип хімічного зв’язку та намалюйте структурну та електрону формули його вищого оксиду. |
9 клас
Хімія
Опрацювати пар. 6 та 7 , виконати завдання 45 (усно), с. 36 ; завдання 50 (письмово), с.42
Відеодослід “Дисоціація кислот” (див. посилання).
10 клас
Хімія
Опрацювати пар. 31 та 32, виконати завдання 226 та 234 (усно), 229 а ( письмово). Провести домашній експеримент на с. 186.
Відеодослід «Якісна реакція на глюкозу» (див. посилання)



